- 在肥胖症患者中进行的单剂量递增(SAD)研究中,ASC30口服片显示出与剂量成比例的(dose-proportional)药代动力学(PK)特征,半衰期(t1/2)长达60小时,支持每日一次或更低频率的口服给药。
-ASC30口服片整体安全性和耐受性良好。所有不良事件(AE)均为轻度(1级)或中度(2级),大部分AE与胃肠道(GI)相关。无3级或以上AE,也无严重不良事件(SAE)。丙氨酸氨基转移酶(ALT)、天冬氨酸氨基转移酶(AST)和其它肝酶均在正常范围内。
-ASC30口服片在室温下稳定。ASC30片在动物模型中的相对口服生物利用度达99%。
-ASC30新片剂在动物模型中的数据支持更低频率的口服给药,或可达一周一次。
-ASC30口服片每日一次治疗肥胖症患者的美国Ib期多剂量递增(MAD)研究的减重、安全性和PK等顶线结果预计于2025年3月底公布。
中国香港,2025年1月21日--歌礼制药有限公司(香港联交所代码:1672,“歌礼”)今日宣布ASC30口服片治疗肥胖症患者(体重指数(BMI):30-40 kg/m2)的美国单剂量递增(SAD)研究(NCT06680440)取得积极顶线结果。该SAD研究由5个队列(2毫克、5毫克、10毫克、20毫克和40毫克)组成,共计40名肥胖症患者,于空腹状态下进行。
在肥胖症患者中进行的SAD研究中,ASC30口服片显示出与剂量成比例的(dose- proportional)药代动力学(PK)特征,半衰期(t1/2)长达60小时,支持一日一次或更低频率的口服给药。跨试验比较(cross-trial comparison)表明,在人体中,5 毫克 ASC30 单剂量的药物暴露量(曲线下面积,“AUC”)是 6 毫克 orforglipron 单剂量的 2.2 倍[1]。与其它在研小分子口服GLP-1受体(GLP-1R)激动剂相比,ASC30口服片显示出更优越的PK特征(包括更长的t1/2和更高的AUC)[1-3],这意味着ASC30口服片有望成为治疗肥胖症的同类最佳小分子GLP-1R激动剂。
队列5中,肥胖症患者在空腹和进食状态下均口服单剂量 40 毫克 ASC30 口服片。数据显示,ASC30口服片的PK特征(包括AUC和t1/2)在空腹和进食状态下基本相同,这表明ASC30口服片服用方便,可每日一次口服给药,不受食物和水的影响。
ASC30口服片在Ia期SAD研究中整体安全性和耐受性良好。所有不良事件(AE)均为轻度(1级)或中度(2级),大部分AE与胃肠道(GI)相关。无3级或以上AE,也无严重不良事件(SAE)。ASC30口服片的GI相关安全性特征与其它在研小分子口服GLP-1R激动剂一致或更佳[1,3,4] (表1)。此外,丙氨酸氨基转移酶(ALT)、天冬氨酸氨基转移酶(AST)和其它肝酶均在正常范围内。
表1. ASC30口服片所有GI相关AE均为轻度(1级)或中度(2级)
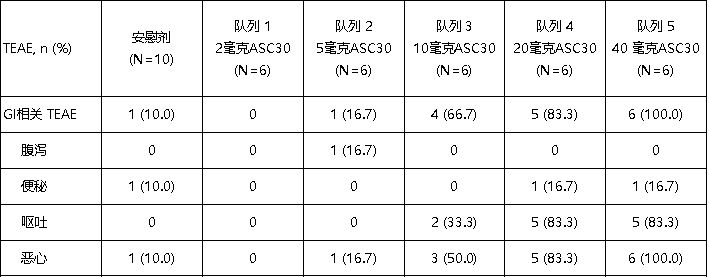
| TEAE:治疗期出现的不良事件;GI:胃肠道; n:每个剂量组发生GI相关不良事件的患者人数;N:接受试验用药品的患者人数。 |
ASC30口服片剂利用歌礼专有技术研发而成,室温下稳定,稳态相对口服生物利用度在动物模型中达99%。ASC30新片剂(室温下稳定)在动物模型中的数据支持更低频率口服给药,或可达一周一次。
ASC30 是歌礼自主研发的不募集β-抑制蛋白(without β-arrestin recruitment)的小分子GLP-1R偏向激动剂(GLP-1R biased small molecule agonist)。ASC30 具有独特和差异化性质,使得每月一次皮下注射和每日一次口服给药均成为可能。经过头对头比较,ASC30 对 GLP-1R 的体外药效比orforglipron高出2到3倍。在对非人灵长类动物(NHPs)进行的静脉葡萄糖耐受实验(IVGTT)中,经过头对头比较,与orforglipron(剂量:6 毫克/公斤)相比,ASC30(剂量:1.5 毫克/公斤)刺激分泌的胰岛素更多,具有统计学显著性差异。
ASC30是首款也是唯一一款既可每月一次皮下注射也可每日一次口服治疗肥胖症的小分子GLP-1R激动剂。基于其PK和安全性特征以及对GLP-1R 的激动作用,ASC30口服片有望成为同类最佳的 GLP-1R 小分子激动剂。
“ASC30口服每日一次治疗肥胖症患者的Ia期SAD研究结果展现出了同类最佳的潜力,对此我们非常激动。我们在SAD研究中已观察到了ASC30优越的PK特征,期待在今年三月底分享在肥胖症患者中进行的Ib期28天多剂量递增试验的药效、安全性和PK数据。”歌礼创始人、董事会主席兼首席执行官吴劲梓博士表示,“ASC30作为一种小分子药物,有望提供每日一次口服和每月一次皮下注射两种给药选择。”
ASC30口服片美国Ib期MAD研究进展
ASC30口服片MAD研究由3个队列组成,每周剂量递增(weekly titrations),肥胖症患者每日一次接受ASC30片或安慰剂给药,为期28天。队列1(2毫克、5毫克、10毫克和20 毫克)已完成,队列2 (2毫克、10毫克、20毫克和40 毫克)和队列 3 (5毫克、15毫克、30毫克和60毫克)将分别于2025年2月下旬和3月下旬完成。MAD研究顶线结果的减重、安全性和PK等数据预计将于2025年3月底公布。
ASC30口服片治疗肥胖症的美国Ia和Ib期临床研究
ASC30口服片Ia期研究(每日一次)是一项随机、双盲、安慰剂对照、单剂量递增(5个队列)的研究,旨在评估ASC30片在肥胖症患者(BMI:30-40 kg/m2)中的安全性、耐受性和PK。
ASC30口服片Ib期研究(每日一次)是一项随机、双盲、安慰剂对照、多剂量递增(3个队列,每周剂量递增,每日一次,为期28天)的研究,旨在评估ASC30片在肥胖症患者(BMI:30-40 kg/m2)中的安全性、耐受性、PK和疗效。
关于 ASC30
ASC30是一款正在临床研究中的小分子GLP-1R偏向激动剂,具有独特和差异化性质,使得同一小分子同时适用于皮下注射和口服片剂给药成为可能。ASC30是一种新型分子实体(NME),拥有美国和全球化合物专利保护,专利保护期至2044年。
参考资料
1.Diabetes Obes Metab. 2023; 25:2634–2641.
2.Obesity 2024: Volume 32, Issue S1, Poster 342.
3.Obesity 2024: Volume 32, Issue S1, Poster 219.
4.Diabetes 2023: Volume 72, Issue Supplement_1, Poster 754.
关于歌礼制药有限公司
歌礼是一家在香港证券交易所上市(1672.HK)的创新研发驱动型生物科技公司,涵盖了从新药研发至GMP生产的完整价值链。歌礼的管理团队具备深厚的专业知识及优秀的过往成就,在团队的带领下,歌礼聚焦两大临床需求尚未满足的医疗领域:代谢性疾病和病毒性疾病,并以全球化的视野进行布局。歌礼的研发管线拥有多款在研药物。
欲了解更多信息,敬请登录网站:www.ascletis.com。
详情垂询:
Peter Vozzo
ICR Healthcare
443-231-0505 (美国)
Peter.vozzo@icrhealthcare.com
歌礼制药有限公司PR和IR团队
+86-181-0650-9129 (中国)
pr@ascletis.com
ir@ascletis.com